중대한 이상 사례 12건 발생
전진숙 "안전성 검증 마련"
[세종=뉴스핌] 신도경 기자 = 치매치료제 레켐비의 국내 부작용이 허가 1년 만에 135건 발생했다.
20일 전진숙 더불어민주당 의원이 식품의약품안전처로부터 제출받은 자료에 따르면, 레켐비의 이상 사례 보고 건수는 2024년 8~12월까지 5개월 동안 12건에서 2025년 1~6월까지 123건으로 10배 이상 늘었다.
건강보험심사평가원의 의약품안전사용서비스에 따르면, 레켐비 처방은 지난해 12월 출시 첫 달 167건에서 올해 8월 2766건으로 급증했다. 9개월 동안 누적 처방 건수는 1만3719건에 달했다.
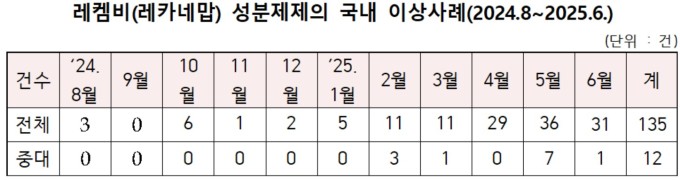
레켐비는 지난해 5월 24일 국내 허가 이후 8월부터 이상 사례가 보고됐다. 지난해 8월 3건이던 보고 건은 10월 6건, 11월 1건, 12월 2건으로 증감을 반복했다. 올해의 경우 1월 5건, 2월 11건, 3월 11건, 4월 29건, 5월 36건, 6월 31건이 추가돼 누적 135건에 이르렀다.
이상 사례 보고 건 중 중대한 이상 사례는 12건으로 집계됐다. 장기적 뇌 손상과 위축을 유발할 수 있는 위험성이 있는 아밀로이드 관련 이상, 혈액 속 철분이 분해돼 조직에 쌓인 색소 침착 부작용 등이 있다.
전 의원은 "미국에서는 이미 임상시험 단계에서 사망 사례가 보고되고 시판 후에도 추가 사망이 3건 발생했다"며 "치매치료제는 국민의 희망이지만 검증되지 않은 희망은 절망이 되는 만큼 식약처는 안전성 검증과 시판 후 조사를 서둘러 부작용을 줄일 수 있는 보완 조치를 마련해야 한다"고 강조했다.
sdk1991@newspim.com























