블루프린트의 표적암 치료제 '아이바키트'
이 기사는 1월 16일 오전 02시01분 '해외 주식 투자의 도우미' GAM(Global Asset Management)에 출고된 프리미엄 기사입니다. GAM에서 회원 가입을 하면 9000여 해외 종목의 프리미엄 기사를 보실 수 있습니다.
[서울=뉴스핌] 김현영 기자 = 월가에서 바이오테크 분야를 집중적으로 다루는 구겐하임 증권의 마이클 슈미트 애널리스트가 앞으로 대형 제약사의 인수 제안을 받을 가능성이 크다고 생각하는 또 다른 생명공학 기업은 신닥스 파마슈티컬스(종목명: SNDX)다.
2005년 10월 설립돼 미국 매사추세츠주 월덤에 소재한 항암제 개발 전문 기업 신닥스 파마슈티컬스는 백혈병 치료 약물 레부메닙(revumenib)과 특발성 폐 섬유증(IPF) 치료제로 개발된 악사틸리맙(axatilimab)에 대해 미국 식품의약국(FDA)에 각각 신약허가신청(NDA)과 생물학적 제재 허가 신청서(BLA)를 제출했다.
레부메닙은 변이형 뉴클레오포스민(mNPM1)과 KMT2A-재배열(KMT2Ar) 재발성/불응성(R/R) 급성 백혈병 치료에 효과가 있는 약물이다. mNPM1 급성 백혈병은 급성 골수성 백혈병(AML)의 일종으로 체내 뉴클레오포스민(NPM1) 유전자에 변이가 생길 때 발생하며, KMT2Ar R/R 급성 백혈병은 KMT2A 유전자에 변이가 생겨 발생한다.
KMT2Ar 급성 백혈병에서 변이된 KMT2A 유전자는 퓨전 단백질을 형성하는데, 퓨전 단백질이 메닌(menin) 단백질과 결합하면 백혈병 암세포의 성장을 촉진한다. 레부메닙은 메닌 억제제의 일종으로 메닌 단백질과 MLL 단백질 복합체 사이의 상호작용을 차단하는 작용을 한다.
콜로니 자극 인자 1(CSF-1) 수용체를 저해하는 단일클론 항체인 악사틸리맙은 2021년 4월 FDA의 '희귀의약품'으로 지정됐다. 중증 만성 폐 질환의 일종인 특발성 폐 섬유증은 폐 조직에 섬유증과 반흔이 나타나는 특성을 보이며, 진단 후 생존 기간이 평균 3~5년 정도로 알려져 있다.
특발성 폐 섬유증 환자들은 숨이 차는 증상의 악화와 만성 기침, 피로, 쇠약, 흉통 등의 증상들을 수반하는데, 현재 시판되는 치료제들은 증상의 진행 속도를 늦출 뿐 멈추게 하지는 못한다. 유일하게 치유력이 있는 요법으로 폐 이식수술이 꼽히지만, 전체 환자들 가운데 실제로 이식수술을 받는 경우가 소수에 불과한 만큼 악사틸리맙이 승인되면 큰 시장이 열릴 것으로 업계 전문가들을 보고 있다.
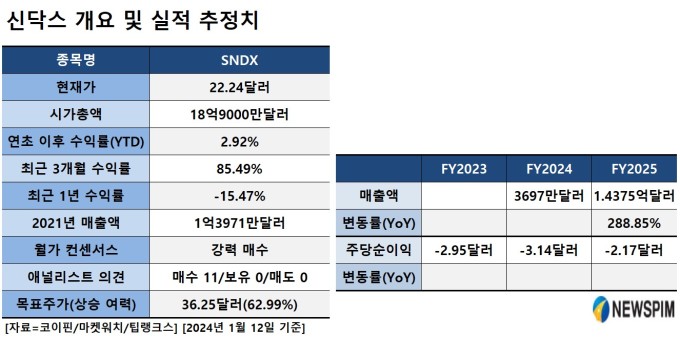
현재 시가총액이 18억9000만달러이고 12일 종가가 22.24달러인 신닥스의 주가는 올해 들어 2.92%, 최근 3개월간 85.49% 뛰었다. 신닥스 역시 월가의 11개 투자은행(IB)이 만장일치로 '매수' 투자의견을 내 '강력 매수' 컨센서스가 형성된 종목이다. 향후 12개월 목표주가 평균은 36.25달러로 12일 종가보다 62.99% 높다.
 |
2008년 10월 설립돼 미국 매사추세츠주 케임브리지에 본사를 둔 정밀의학 치료제 전문 기업 블루프린트 메디슨스(BPMC)도 구겐하임 증권이 피인수 후보로 주목하는 생명공학 기업이다. 블루프린트는 아이바키트(Ayvakit)와 가브레토(Gavreto)로 알려진 두 가지 표적 암 치료제를 성공적으로 개발했으며, 암과 특정 혈액암 치료를 위한 혁신적인 치료법을 개발하는 데 주력하고 있다.
블루프린트의 위장관기질종양(GIST) 치료제 아이바키트는 2021년 6월 FDA가 성인 진행성 전신 비만세포증 치료제 용도로 적응증 추가를 승인한 약물이다. 희귀 혈액 질환인 진행성 전신 비만세포증은 여러 장기의 손상과 생존 기간 감소, 삶의 질 저하가 나타나는 쇠약성 질환이다.
여기서 진행성 전신 비만세포증은 공격성 전신 비만세포증(ASM), 혈액학적 종양과 관련이 있는 전신 비만세포증(SM-AHN) 및 비만세포 백혈병(MCL) 등을 포함하는 개념으로, 전신 비만세포증은 대부분 'D816V 변이 KIT' 유전자에 의해 유발되는 희귀 혈액학적 장애의 일종이다. 아이바키트는 'D816V 변이 KIT' 유전자를 강력하고 선택적으로 저해하도록 설계된 최초의 승인받은 표적 치료제다.
2023년 5월 FDA는 아이바키트를 성인 무통성 전신 비만세포증(ISM) 환자를 위한 최초이자 유일한 치료제로 적응증을 확대해 승인했다. 이는 무통성 전신 비만세포증에 대해 진행된 역대 최대 규모의 연구인 이중맹검, 위약 대조 PIONEER 시험의 데이터를 근거로 승인됐다. 이로써 아이바키트는 진행성 및 무통성 전신 비만세포증 전반에 걸쳐 승인된 유일한 치료제가 됐다.

이에 앞서 아이바키트는 유럽에서 'PDGFRA D842V' 유전자변이를 가진 성인의 절제 불가능 또는 전이성 위장관기질종양 치료제로 승인된 바 있다. 미국에서는 'PDGFRA D842V' 변이를 포함한 'PDGFRA 엑손 18 변이'를 가진 절제 불가능 또는 전이성 GIST 환자의 치료제로 승인돼 아이바키트라는 제품명으로 발매됐다.
성인 무통성 전신 비만세포증 환자를 위한 치료제로 승인받은 후 첫 분기인 지난해 3분기에 아이바키트의 순매출은 전년 동기 대비 90% 증가한 5420만달러를 기록하며 월가 예상치 4500만달러를 크게 웃돌았다. 이중 4910만달러가 미국에서 발생했다.
오펜하이머의 매튜 비글러 애널리스트는 아이바키트의 판매 호조와 향후 추가 성장 전망을 바탕으로 블루프린트에 대한 낙관론을 펼쳤다. 비글러는 "출시에 앞서 아이바키트가 커뮤니티와 진료 센터에 침투할 수 있을지가 가장 우려됐는데, 아직 초기 단계이긴 하나 잘 침투하고 있는 것으로 보이며 앞으로 대상 시장도 크게 늘어날 전망"이라고 진단했다. 이어 오펜하이머의 최대(피크) 매출 추정치를 6억5000만달러에서 10억5000만달러로 상향 조정한다고 밝혔다.
구겐하임의 마이클 슈미트 애널리스트는 블루프린트의 약물에 대해 단기적으로 경쟁 상대가 없을 것으로 보고 있다. 블루프린트에 따르면 지난해 3분기 말 기준 800명 이상의 환자가 아이바키트를 사용하고 있는 것으로 추산된다.
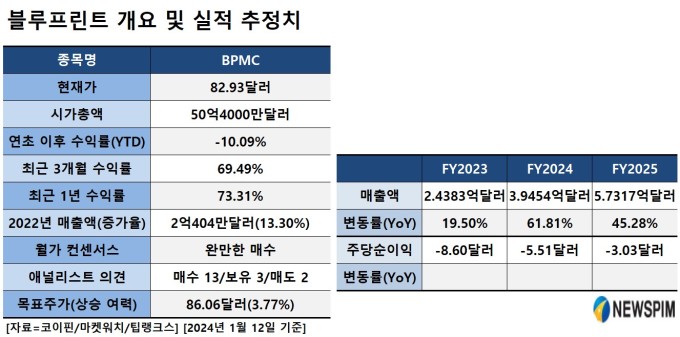 |
현재 시총이 50억4000만달러이고 12일 종가가 82.93달러인 블루프린트는 올해 들어 주가가 10.09% 하락했지만 최근 3개월간 69.49% 상승했다. 월가에선 최근 3개월간 18개 IB 중에서 13곳(72%)이 매수, 3곳이 보유, 2곳이 매도 의견을 제시해 '완만한 매수' 컨센서스가 형성됐다. 목표주가 평균은 86.06달러로 12일 종가에서 3.77% 추가 상승 여력을 나타낸다.
kimhyun01@newspim.com