램시마 美 FDA 판매 승인…3.5조원 매출 기대
[뉴스핌=정탁윤 기자] 김형기 셀트리온 대표는 6일 "보수적으로 잡아도 10년내 전세계 매출 10조원 달성이 가능할 것"이라고 밝혔다.
김 대표는 이날 서울 광화문의 한 호텔에서 열린 '램시마'의 미국 FDA 허가 관련 간담회에서 "셀트리온은 향후 램시마를 비롯 지난해 유럽 허가를 신청한 비호지킨스 림프종 치료제 트룩시마 등을 통해 글로벌 10위권 기업으로 성장해 가겠다"며 이같이 말했다.
 |
| <사진=셀트리온> |
셀트리온은 이날 첫 항체 바이오시밀러인 '램시마(Remsima)'가 미국 식품의약국(FDA)으로부터 미국 내 판매 허가를 획득했다고 밝혔다.
셀트리온은 이번 허가를 통해 미국을 포함해 총 71개 국가에서 램시마를 판매하게 된다. 램시마의 오리지널 제품인 존슨앤드존슨사의 레미케이드는 세계 시장에서 한해 98억 8500만달러(약 12조원)의 매출을 기록하며 전세계 판매액 기준 3위에 오른항체의약품이다.
램시마는 오리지널 제품을 포함해 같은 적응증을 보유한 TNF-알파 억제제 시장에서도 경쟁할 전망이다. TNF-알파 억제제의 세계 시장은 약 35조원 규모이며, 이 가운데 미국 시장은 20조원 규모로 파악되고 있다.
이 시장은 레미케이드(존슨앤드존슨)를 비롯, 휴미라(애브비), 엔브렐(암젠) 등 3개 블록버스터 제품이 분점하고 있다. 향후 램시마가 이 시장의 약 10%를 점유한다고 할때 한 제품만으로 약 3조5000억원의 매출이 가능할 것으로 예상된다.
김 대표는 "국내 90여 상장 제약사 매출 총액이 20조원이 안 되는 한국 제약산업에서 단일품목으로 조 단위 매출을 내는 의약품의 탄생은 큰 의미가 있다"고 강조했다.
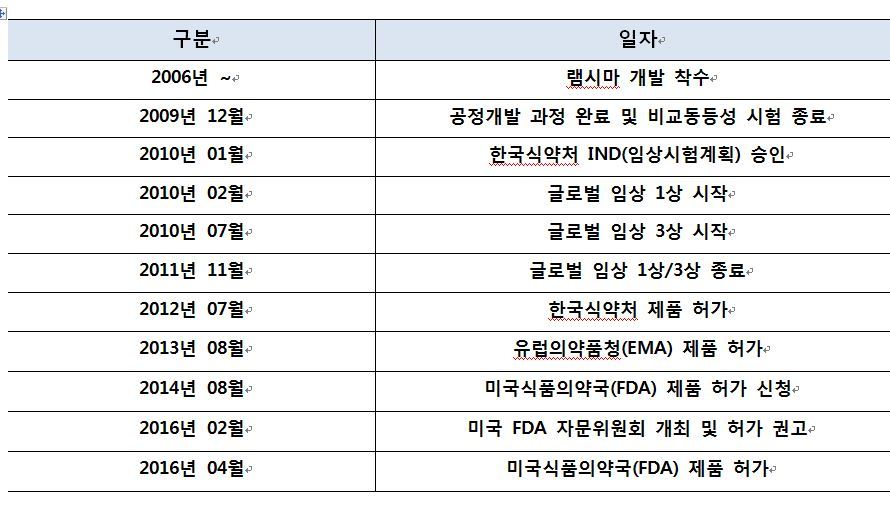 |
| <표=셀트리온> |
허가 이후 램시마의 미국 내 유통은 셀트리온과 북미 유통 독점 계약을 맺은 화이자가 담당한다. 김 대표는 본격 시판 계획과 관련 "여러 절차를 준비하는데 6개월 정도 걸리는데 정확한 시판 시기는 파트너와 상의할 예정"이라며 "조만간 (시판 시기 등) 결정을 위한 미팅을 가질 예정"이라고 설명했다.
셀트리온은 이날 램시마 이후 파이프라인(후속제품)에 대한 계획도 밝혔다. 먼저 한국에서 이미 허가를 받은 유방암치료제인 허셉틴 바이오시밀러 '허쥬마'의 조기유방암 임상을 추가로 진행, 올해 하반기 중 글로벌 허가에 돌입할 예정이다.
또한 지난해 10월 비호지킨스 림프종 치료제인 리툭산 바이오시밀러 '트룩시마'가 국내 및 유럽 허가 절차에 돌입해 판매 허가 승인을 기다리고 있다.
바이오시밀러 외에 항체 기술을 기반으로 한 신약 개발도 진행 중이다. 종합인플루엔자 항체 치료제인 CT-P27은 개발을 완료하여 임상 2a상을 완료했으며, 항체바이오의약품과 화학의약품을 링커로 결합한 유방암 치료용 바이오베터(Bio-Better)인 CT-P26은 비임상 완료 후 임상을 준비 중이다.
[뉴스핌 Newspim] 정탁윤 기자 (tack@newspim.com)
 영상
영상