블루오션 시장에 호재…당장 내년에는 효과 미미
[서울=뉴스핌] 방보경 기자 = 내년부터 희귀질환 치료제 보험등재 절차가 줄어든다. 신약을 개발하는 제약사들은 제품 출시가 빨라져 긍정적인 영향을 받을 것으로 보인다. 다만 화이자를 제외하고는 임상 초기 단계에 있는 파이프라인이 많아 가까운 시일 내에 수혜를 입기란 어렵다.
23일 업계에 따르면 내년 1월 1일자로 중증 희귀질환 치료제·항암제 보험등재 절차가 2개월 단축된다. 건강보험심사평가원에서 30일, 건강보험공단에서 30일을 단축하는 것이다. 보험등재 절차는 6개월이 원칙이지만, 업계에서는 통상적으로 6개월에서 1년 정도 걸려 빠른 시장 진입에 어려움을 겪었다.
보건복지부의 결정은 최근 들어 시장이 커지고 있는 희귀질환 치료제에는 호재다. 제약업계에서는 희귀질환 치료제가 '블루오션'으로 부상하고 있다. 임상 환자가 적어 유효성을 확보하기 어렵다는 한계는 있지만 누구도 뛰어들지 않은 영역을 선점하면 큰 이익을 얻을 수 있을 거라는 분석이다. 제약 쪽 후보물질은 충분히 개발됐다는 위기 의식도 희귀질환 치료제의 매력을 더했다.

희귀질환 치료제 시장에 뛰어드는 기업은 늘고 있다. 한미약품, 녹십자, 종근당 등이 현재 희귀질환 치료제 신약 임상을 진행하고 있다.
한미약품은 선천성 고인슐린증 HM15136, 단장증후군 HM15912, 성장호르몬 결핍중 에페소마트로핀이 임상 2상에 들어섰다.
GC녹십자는 파트너사를 통해 희귀질환 치료제를 개발 중이다. 추후 개발이 완료되면 판권을 들여올 예정이다. 그중에서도 'SSADHD(숙신알데히드 탈수소효소 결핍증)' 치료제는 FIC 혁신신약에 속한다. SSADHD는 유전자 결함에 따른 효소 부족으로 인해 열성 유전되는 신경퇴행성 질환이다.
종근당은 샤르코-마리-투스 치료 신약 'CKD-510'의 유럽 임상 1상을 마쳤고, 현재 미국 임상 1상을 진행 중이다. 내년 초 글로벌 2상을 진행할 것으로 예상된다. 헌팅턴증후군 신약 CKD-504는 임상 1상을 마친 상태다.
단 국내 제약업체들은 가까운 시일 내에 수혜를 입기는 어렵다는 입장이다. 대부분의 파이프라인은 임상 초기이기 때문에 내년에 개발을 마치기 힘들다.
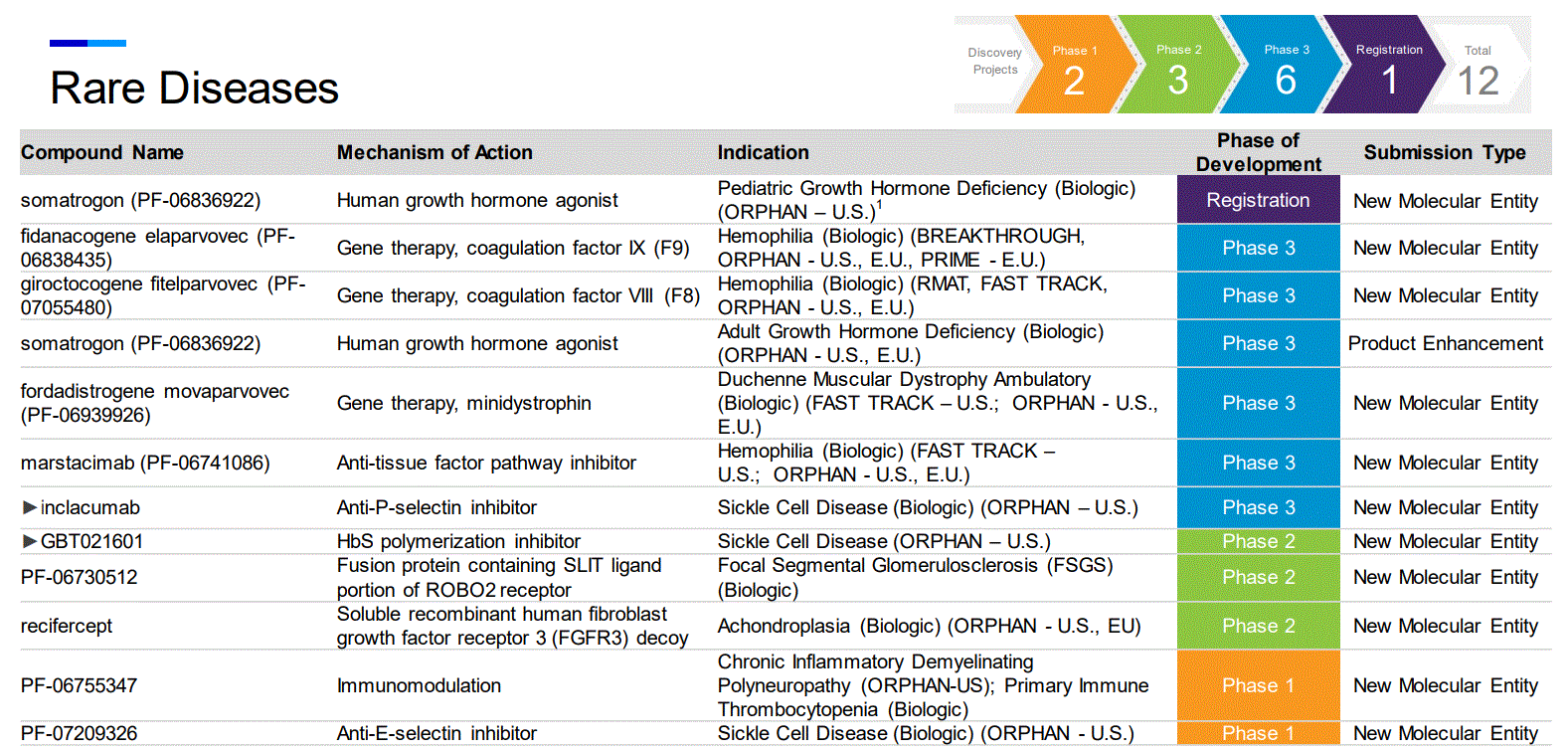
내년에는 화이자 희귀질환 치료제들이 영향을 받을 것으로 추측된다. 희귀약 중 임상을 끝낸 제품들은 빈다맥스와 엔젤라로 총 2개다. 빈다맥스는 건강보험 급여 절차를 진행 중이며, 엔젤라는 내년 초 허가를 받기 위해 준비하고 있다.
빈다맥스는 ATTR-CM 치료 옵션이다. ATTR-CM은 적절한 치료를 받지 못할 경우 생존 기간이 2년에서 3년 6개월에 그치나 빈다맥스 외에는 마땅한 치료제가 개발되지 않았다. 보건복지부는 대체약이 없을 경우에 한해 등재 절차를 줄인다고 했기에 기간이 단축될 가능성이 있다. 엔젤라는 소아 성장호르몬 결핍 치료제다.
한국화이자제약 관계자는 "정부에서 발표한 기준에 따라 혜택을 볼 수 있을지는 확실치 않다"며 "내년 1월부터 변경되는 만큼 확인해봐야 할 것"이라고 전했다.
hello@newspim.com























