[세종=뉴스핌] 이경화 기자 = 식품의약품안전처가 국내 혁신 의료제품 개발 지원을 위해 '글로벌 혁신제품 신속심사 지원(GIFT) 프로그램'을 본격화하며, 13일 '의약품 신속검사 보고서'를 발간했다.
GIFT 프로그램은 글로벌 혁신 의료제품이 빠르게 제품화될 수 있도록 개발(임상) 초기부터 지원하는 프로그램이다.
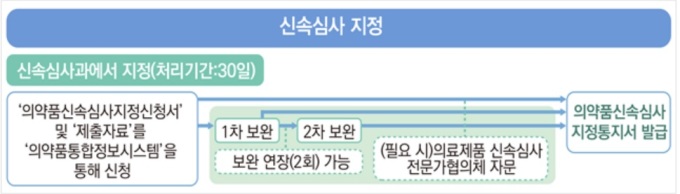
식약처는 제약업체가 신속심사 대상 신청 시 지정을 검토하고, 필요할 경우 의료제품 신속심사 전문가협의체 자문을 거쳐 GIFT 대상을 결정한다.
GIFT 대상은 ▲준비된 자료부터 먼저 심사하는 수시 동반심사(rolling review) 적용 ▲품목설명회·보완설명회 등 심사자와 개발사 간 긴밀한 소통 ▲규제 관련 전문 컨설팅 ▲혁신성(안전성·유효성 개선)이 뛰어난 제품은 임상 결과 등을 제공해 국내 의약품 개발 독려 ▲안전과 직접 관련 없는 일부 자료는 시판 후 제출 ▲ICH 등 글로벌 심사기준 선제적 적용 등의 지원을 받게 된다.
이날 발간한 보고서는 GIFT 프로그램의 일환으로 식약처가 지난 2년간 신속 심사한 경험을 기반으로 작성했다. 주요 내용으로 ▲2020년 8월31일~2022년 7월31일 의약품에 대한 신속심사 지정 현황 ▲신속검사로 허가된 의약품 ▲신속검사 지정 사유와 제품의 임상 결과가 담겼다.
식약처 관계자는 "앞으로도 국내 의약품 업계의 혁신제품 연구·개발을 지원하기 위해 국내 신속검사 현황과 분석 정보를 지속해서 제공하겠다"고 했다.
kh99@newspim.com























