[서울=뉴스핌] 정경환 기자 = 셀리버리는 개발 중인 내재면역제어 코로나19 면역치료제 'iCP-NI'가 코로나19 바이러스(SARS-CoV-2) 감염 영장류모델에서, 피 혈장뿐만 아니라 폐 기관지에서 촉발되는 싸이토카인스톰(면역폭풍)까지도 억제한다는 결과를 서던리서치로부터 수령했다고 26일 밝혔다.
회사 측은 "이번 분석보고서는 원숭이 2차효능평가시험 중 마지막 분석데이터"라며 "최종 시험종료보고서를 수령하는 즉시 글로벌 임상대행사 코방스에 전달해 미국에서의 임상시험계획 파일링(FDA IND Filing)이 될 것"이라고 했다.
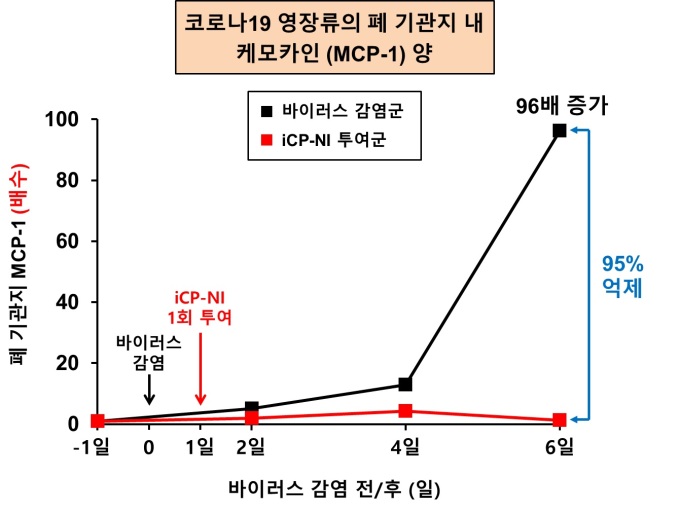
셀리버리에 따르면, iCP-NI는 코로나19 감염 영장류의 혈장 내 싸이토카인폭풍 억제효능(인터페론-감마 66% 감소, 인터루킨-2 110% 감소, MCP-1 93% 감소)뿐만 아니라, 코로나19 감염 시 바이러스에 가장 먼저 노출되고, 가장 심각한 염증이 발생하는 부위인 폐 조직에서도 면역폭풍을 억제(95%)한다는 것이 밝혀졌다.
이로써 코로나19 감염으로 발생하는 전신염증 및 직접 감염기관인 호흡기의 폐렴까지 제어하는 코로나19 면역치료신약으로서의 확실한 증거를 확보했다는 설명이다.
이에 따라 셀리버리는 코로나19 영장류 치료효능 평가시험을 더 이상 하지 않아도 미국에서 임상시험을 추진하기에 충분하다고 하는 코방스 측의 의견을 받아들여 추가 원숭이 시험을 하지 않고 임상시험계획서를 파일링할 계획이다.
조대웅 셀리버리 대표는 "지난 22일, 미국 식품의약국(FDA)이 에볼라 바이러스 복제 억제제로 개발하던 렘데시비르를 코로나19 치료제로 승인함에 따라 셀리버리의 iCP-NI가 구제의약품 및 긴급치료목적사용승인 제도로 개발되는 것에 대한 우려가 있다"며 "이는 매우 잘못된 가짜뉴스"라고 했다.
그는 이어 "이전의 팬데믹 상황 또는 적절한 치료제가 없는 상황에서 환자들에게 FDA는 여러 종류 약물의 치료목적사용승인 신청을 받아들인 바 있고, 실제 그런 제도로 많은 약물이 제약시장에 등장해 왔다"며 "iCP-NI를 긴급치료목적사용승인 제도로 최단기간 내 개발하는 데 전혀 무리가 없다"고 강조했다.
조 대표는 그러면서 "현재 코로나19 감염 영장류 효능평가와 코로나19와 같은 RNA 바이러스 감염성 폐렴으로 죽는 동물모델에서의 생명을 살리는 치료효능 평가시험에서 효능이 모두 증명되고 있다"며 "실제 임상대행사인 코방스 측도 데이터가 충분하다고 평가했다"고 덧붙였다.
hoan@newspim.com