대장암·췌장암·골육종 치료제 임상 순항
골육종 치료제, 미국 FDA서 ODD·RPDD 지정
이 기사는 9월 15일 오후 3시35분 AI가 분석하는 투자서비스 '뉴스핌 라씨로'에 먼저 출고됐습니다.
[서울=뉴스핌] 배요한 기자 = 메드팩토가 신속 승인이 가능한 암종(대장암·췌장암·골육종)에 대한 임상에 집중하는 '선택과 집중' 전략을 통해 미국 식품의약품(FDA) 신약 허가에 속도를 내고 있다. 최근 골육종 환자 대상 백토서팁 단독 요법은 미 FDA 1/2상 임상시험계획(IND) 승인을 받은 데 이어 희귀 소아질환 의약품(RPDD)으로 지정됐다. 지난해 이 치료제는 FDA로부터 희귀의약품 지정(ODD)을 받기도 했다.
과거 메드팩토는 파이프라인 백토서팁을 모든 암종으로 적응증을 확대하고 병용투여 임상에 나섰지만, 치료제의 조기 상용화를 목표로 적응증 임상을 3개로 줄이는 과감한 결단을 내린 바 있다.
메드팩토 관계자는 15일 "신속승인 절차를 통해 최대한 빠르게 미 FDA 승인을 받을 수 있는 임상에 집중하고 있다"며 "과거 7개의 암종을 대상으로 임상을 진행했지만 올해부터 대장암, 췌장암, 골육종 3개 암종에 대한 임상 개발에 박차를 가하고 있다"고 밝혔다.
또한 "골육종 치료제가 FDA 희귀의약품과 소아희귀질환 치료제로 지정받은 만큼 신약 허가 절차가 빨라질 것으로 기대한다"고 덧붙였다.
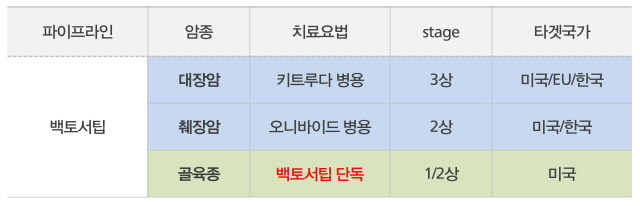
가장 임상 진척이 빠른 메드팩토의 대장암 치료제는 키트루다 병용요법으로 미국, 유럽, 한국을 타겟으로 임상 3상을 준비 중이다. 임상시험은 약 300명의 진행성 대장암 환자를 대상으로 진행한다. 회사 측은 이중 100명의 환자에게서 유의미한 초기 데이터가 도출된다면 FDA 신속승인을 신청한다는 계획이다.
신효섭 DB금융투자 연구원은 "MSS형 대장암은 키트루다 반응률이 없는 암종이기 때문에 병용요법 결과에 대한 관심이 높다"면서 "이번 임상은 머크가 키트루다를 무상 제공하는데, 현재까지 3상 지원 사례는 13건 밖에 없고 MSS형 대장암 적응증으로는 첫 사례여서 의미가 있다"고 설명했다.
췌장암은 백토서팁과 폴폭스(FOLFOX) 및 오니바이드 병용요법으로 임상을 진행 중이다. 전날 메드팩토는 췌장암 관련 백토서팁 병용요법 임상 중간데이터를 미국암연구학회 췌장암 특별 콘퍼런스에서 포스터 발표하기도 했다.
회사 관계자는 "이번에 공개된 임상 데이터는 췌장암 환자에서 백토서팁과 폴폭스 병용요법이 기존 치료 요법 대비 월등한 치료 효과가 있음을 확인했다"고 강조했다.
메드팩토는 올해 안에 백토서팁과 5FU/LV/오니바이드 병용요법에 대한 허가목적 임상 1/2상을 미국 FDA에 신청할 예정이다. 또한 내년 1월 개최되는 미국 임상종양학회 위장관종양 심포지엄(GIASCO)에서는 백토서팁과 오니바이드 병용요법에 대한 임상1b(연구자임상) 중간데이터를 공개한다는 계획이다.

골육종 환자 대상 백토서팁 단독요법은 미국 1/2상을 진행 중이다. 재발 난치성 또는 진행성 골육종을 앓고 있는 14세 이상의 청소년 및 성인 환자들 대상으로 안전성과 효과를 확인하게 된다.
골육종 단독요법은 미 FDA로부터 희귀의약품 뿐만 아니라 희귀 소아질환 의약품으로 지정돼 골육종 치료제로서의 개발이 탄력 받을 것으로 전망된다. 메드팩토는 지난 7월 재발 난치성/진행성 골육종 환자 대상 백토서팁 단독 요법 1/2상 IND를 FDA에 신청하고 한 달만에 승인을 받았다.
신효섭 DB금융투자 연구원은 "메드팩토는 백토서팁 물질에 대한 우려가 있었으나 기타 적응증 임상 승인과 AACR에서 췌장암 대상 우수한 데이터를 도출하며 이상 없음을 간접적으로 증명했다"며 "이제는 R&D 성과에 대한 관심이 필요한 시점"이라고 판단했다.
이어 "내년 1분기 기대되는 이벤트로는 ▲백토서팁/키트루다 병용요법 MSS형 대장암 임상 3상 IND 신청 ▲백토서팁/오니바이드/5FU/LV 병용요법 췌장암 임상 2상 결과 ▲BAG2 항체치료제 임상 1상 IND 신청 등이 예존재한다"고 말했다.
yohan@newspim.com
























