[서울=뉴스핌] 정경환 기자 = 올해 국내 코로나19 진단시약 수출 규모가 2조5000억 원에 이르는 것으로 나타났다. 이는 코로나19를 계기로 새롭게 창출된 것으로, 정부는 이른바 'K-방역'의 성과로 평가하고 있다.
식품의약품안전처는 국내 코로나19 진단시약이 지난달 30일 기준으로 전 세계 170여개 국가로 총 4억9679만 명분이 수출됐다고 4일 밝혔다.
국내 코로나19 진단시약 가운데 수출용 제품으로 허가된 것은 현재 221개 제품(유전자 105, 항원 44, 항체 72)이다.
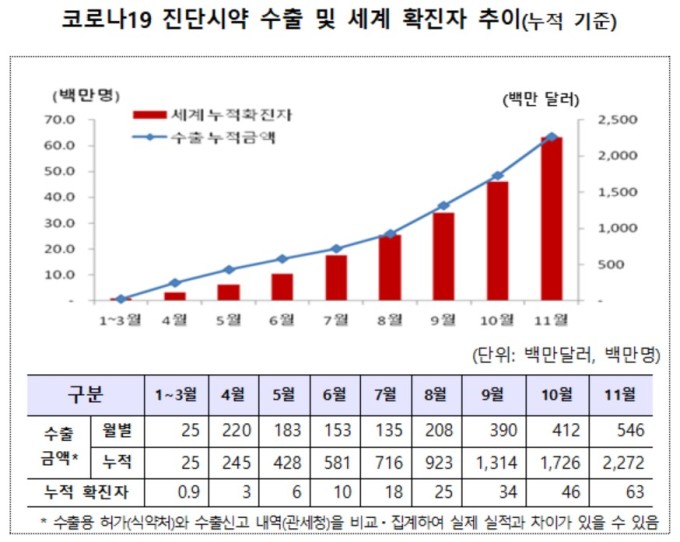
관세청에 따르면, 올해 초부터 11월까지 코로나19 진단시약의 총 수출금액이 약 2조5000억 원(22억7000만 달러)으로 수출이 급증하고 있다.
지난 4월부터 본격적으로 시작된 수출은 7월 이후 확진자 급증에 따라 가파른 상승세를 보였으며, 10월과 11월에 연이어 수출 최고치(월별 기준)를 경신했다.
수출 국가별로 보면, 인도가 15.6%로 비중이 가장 컸다. 이어 독일(13.2%)과 네덜란드(9.6%), 이탈리아(7.8%) 그리고 미국(5.2%) 순이다. 이들 상위 5개 국가가 전체 수출액의 50% 이상을 차지했다.
수출 국가도 올해 1~3월 83개 국가에서 11월까지 총 170여 개 국가로 지속 확대됐다.
식약처는 현재(12월 3일 기준)까지 국내 코로나19 진단 등을 위해 총 9개(유전자 7개, 항원 1개, 항체 1개) 제품을 정식허가했다.
유전자 진단시약은 코로나19 감염자 확진을 위한 제품(6개)과 기침, 인후통 및 발열 등 증상이 비슷해 구분이 쉽지 않은 코로나19와 인플루엔자를 동시에 진단할 수 있는 제품(1개)이 있다. 또한, 유전자 진단에 비해 정확도는 부족하지만 신속하게 바이러스 유무를 확인할 수 있는 항원 진단시약 1개와 코로나19 바이러스에 대한 항체 존재 여부를 확인할 수 있는 항체 진단시약 1개가 있다.
아울러 정식허가를 신청한 진단시약은 유전자 진단시약 18개, 항원 진단시약 7개, 항체 진단시약 15개로 총 40개 제품이 심사 중에 있다.
국내 방역에 사용 중인 코로나19 진단시약의 1일 최대 생산량은 약 59만 명분이다. 지금까지 558만 명분을 생산해 이 중 475만 명분이 공급됐고, 총 313만 건의 검사(질병관리청 통계)를 진행했다.
식약처 측은 "현재 확보된 재고 약 83만 명분은 최근 일주일 동안 1일 평균 검사량 2만 명분을 감안했을 때 약 한 달 이상 의료현장에 공급할 수 있는 물량"이라며 "안정적인 수급을 이어가고 있다"고 했다.
한편, 우리나라가 제안한 코로나19 등 감염병 진단기법이 국제표준화기구(ISO)의 국제 표준(International Standard)으로 지난 2일 제정됐다.
표준 감염병 진단기법은 '유전자 증폭방식'의 체외진단검사를 수행하는 검사실의 운영절차 및 방법을 정의한 것이다. 코로나19 진단키트에 적용된 실시간 유전자 증폭기법(Real Time Polymerase Chain Reaction) 등 다양한 감염병 진단검사에 적용할 수 있는 표준이다.
식약처 측은 "이로써 향후 국내 진단시약의 국제 신뢰도가 한층 향상되고 국산 체외진단의료기기의 해외시장 확대에도 추진력을 받을 것으로 기대된다"고 했다.
식약처와 관세청은 앞으로도 코로나19 진단시약의 허가부터 수출까지 현황 등을 지속적으로 모니터링, 품질이 우수한 제품의 신속 개발·허가를 적극적으로 지원하고 새롭게 창출된 해외시장에서 'K-진단시약'의 경쟁력이 지속될 수 있도록 노력할 방침이다.
hoan@newspim.com























