뇌 면역세포 기능회복효과 확인
[서울=뉴스핌] 김영섭 기자 = 뇌 면역세포인 미세아교세포의 대사 조절을 통한 알츠하이머병 치료 가능성이 열렸다.
서울대 의과대학 생화학교실 묵인희 교수 연구팀은 알츠하이머병에서 미세아교세포의 대사조절 기전을 발견, 이의 조절을 통한 치매 예방 및 치료 가능성을 확인했다고 28일 밝혔다.
연구결과(논문명 “A breakdown in metabolic reprogramming causes microglia dysfunction in Alzheimer’s disease”)는 세계적 학술지 셀(Cell) 자매지인 ‘셀 메타볼리즘(Cell Metabolism)’에 이날 게재됐다.
알츠하이머병은 노인성 치매의 약 70%를 차지한다. 이 병은 뇌 실질에 비정상적으로 축적되는 베타 아밀로이드 단백질에 의해 신경세포가 손상됨으로써 기억력을 포함한 인지기능이 악화하는 만성 퇴행성 신경질환이다.
또 뇌 면역세포인 미세아교세포는 평상시 주변을 탐지·보수하는 신경교세포인데, 베타 아밀로이드 단백질을 감지하면 활성화해 베타 아밀로이드 단백질을 포식·분해하는 한편, 신경독성을 일으키는 사이토카인을 분비하는 것으로 알려져 있다.
미세아교세포의 이질적인 특성과 기능에 대해서는 많은 연구결과들이 있지만, 알츠하이머병에서의 미세아교세포의 정확한 역할과 기전은 지금까지 알려진 바가 없다.
연구팀은 미세아교세포가 에너지를 생성하는 대사시스템을 실시간으로 확인함으로써 알츠하이머병에서 미세아교세포의 보다 근원적인 생리적 역할을 규명했다.
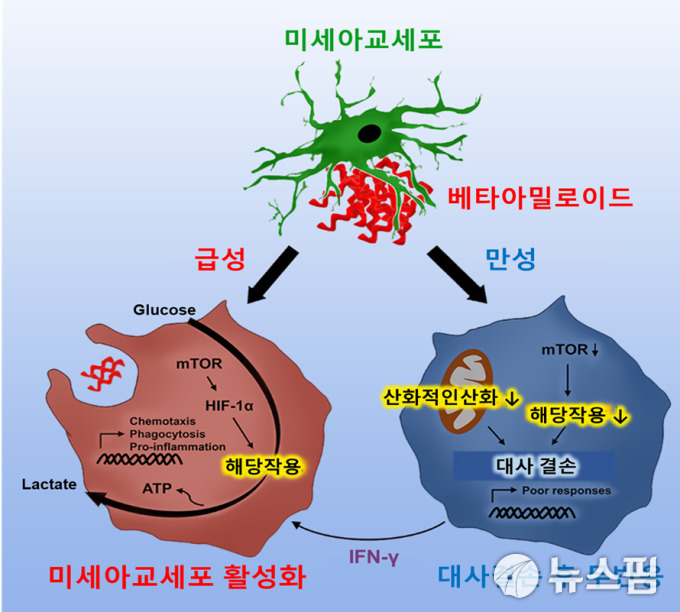
실험결과, 베타 아밀로이드 단백질에 급성으로 노출된 미세아교세포는 에너지대사기전이 에너지생성 속도가 느린 미토콘드리아의 산화적 인산화(燐酸化)에서 에너지생성 속도가 빠른 해당(解糖)과정으로 이동하는 대사재편성(metabolic reprogramming)을 보였다.
또한 이런 대사재편성을 통해 단백질 포식작용과 같은 면역기능이 활성화하는 것이 확인됐다.
반면, 만성적으로 베타 아밀로이드에 노출된 치매 뇌 조직에서 미세아교세포는 산화적 인산화와 해당과정이 모두 손상된 대사결손 상태에 이르고 면역기능장애가 발생함을 발견했다.
이에 연구진은 대사촉진기능이 알려진 감마인터페론을 유전자변형 치매 마우스에 처리하여 대사결손 상태였던 미세아교세포의 해당과정을 회복시켜 면역기능을 활성화, 그 결과 아밀로이드 단백질이 줄어들고 인지능력 또한 회복됨을 확인했다.
이번 연구결과는 알츠하이머병에서 뇌 면역세포인 미세아교세포의 역할과 베타 아밀로이드에 대한 대사학적 반응기전을 확인, 미세아교세포의 대사촉진을 통해 신경퇴행성 질환의 새로운 치료 전략을 제시한 것으로 평가된다.
kimys@newspim.com























