한미·종근당 신약 개발 선도..유한ㆍ대웅도 가세
[편집자] 이 기사는 5월 8일 오후 3시8분 프리미엄 뉴스서비스'ANDA'에 먼저 출고됐습니다. 몽골어로 의형제를 뜻하는 'ANDA'는 국내 기업의 글로벌 성장과 도약, 독자 여러분의 성공적인 자산관리 동반자가 되겠다는 뉴스핌의 약속입니다.
[뉴스핌=한태희 기자] 국내 제약사의 신약 개발이 다시 활기를 띠고 있다. 올 들어 정부가 승인 허가를 낸 의약품 임상시험이 부쩍 증가하는 등 '제 2의 한미약품'을 노리는 제약사들이 늘고 있다.
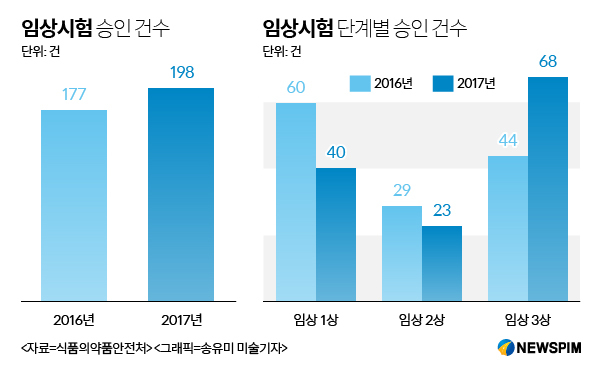
8일 식품의약품안전처 임상시험 승인 현황을 분석한 결과 지난 1~4월중 임상시험 승인 건수는 198건으로 지난해 같은 기간(177건)과 비교해 11.8% 증가했다. 임상시험(전임상·1상·2상·3상)은 환자들을 대상으로 연구가 끝난 약의 효과를 검증하는 단계로, 신약을 개발하는 제약사가 밟아야 할 필수 코스다.
임상시험 승인이 늘었다는 것은 제약사가 신약 개발에 속도를 내고 있다는 의미다. 실제 의약품 출시 전 마지막 단계라고 볼 수 있는 임상 3상 승인이 올해 들어 증가했다.
지난 4개월간 임상 3상 승인은 68건으로 지난해 같은 기간(44건)과 비교해 54.5%나 늘었다. 반면 약 개발 초기 단계에 해당하는 임상 1상은 지난해 60건에서 올해 40건으로 33.3% 줄었다.
 |
한미약품 관계자는 "올리타 국내 임상 3상을 승인받아 개발을 계속한다"고 말했다. 이어 "지난해 제넨텍에 기술을 수출한 표적항암제 신약 'HM95573' 국내 임상 1상 승인도 받았다"며 "신약 개발 진행 상황은 홈페이지에서 전부 공개하고 있다"고 설명했다.약 개발을 주도하는 제약사는 한미약품이다. 한미약품은 올해 식약처로부터 임상시험 4건을 승인받았다. 한미약품은 특히 지난달 13일 폐암 신약 '올리타' 임상 3상 허가를 받았다. 올리타는 한미약품이 독일 제약사 베링거인겔하임에 기술 이전을 했다 지난해 개발 권한을 반환받은 신약 후보군이다. 올리타 안전성 논란도 있었지만 한미약품은 임상 3상에서 불안감을 종식한다는 목표다.
종근당 또한 올해 들어 4개월간 임상시험 4건을 허가받았다. 종근당은 녹내장 개량신약(CKD-351, 2상) 등의 연구를 이어가고 있다. 이외 유한양행과 대웅제약이 각각 임상시험 승인 3건이 뒤를 잇는다. 대웅제약은 턱밑 지방 치료제인 'DWJ211' 임상 2b상 승인을 받아 연구를 이어가는 중이다.
제약업계 관계자는 "지난해 하반기에 신약 개발 열기가 주춤한 상황에서도 제약사가 연구를 이어가 3상 단계에 진입한 것으로 보인다"고 말했다. 다만 "임상시험 승인 건수를 보고 연구 실적을 판단하기가 어렵다"고 덧붙였다.
[뉴스핌 Newspim] 한태희 기자 (ace@newspim.com)























