[서울=뉴스핌] 박다영 기자 = 메지온이 오는 5월말 미국 식품의약국(FDA)에 단심실증 치료 후보물질 '유데나필'의 신약허가신청(NDA)을 할 계획이다.
메지온은 30일 홈페이지를 통해 "NDA 신청시기는 5월 말로 예상하고 있고 FDA가 승인을 위해 요청한 핵심자료를 구비했기 때문에 승인 확률은 더 올라갔다고 판단한다"라고 밝혔다.
단심실증은 심장을 이루는 좌심실과 우심실 중 선천적으로 한 개가 없는 희귀질환이다. 유데나필은 단심실증으로 우심방-폐동맥 우회수술(폰탄수술)을 받은 청소년 환자의 심장과 운동기능을 개선하는 단심실증 치료 후보물질이다.
유데나필은 지난해 11월 공개한 탑라인 데이터에서 환자의 최대 운동 상태에서 최소 산소소비량을 측정한 1차 지표 'Max VO2'이 통계적 유의성을 입증하지 못했지만, 유산소에서 무산소 운동으로 바뀌는 시점에 측정한 산소 소비량을 측정한 2차 지표 'VO2 VAT'는 통계적으로 유의한 결과를 보였다.
메지온에 따르면 회사는 단심실 환자에게 가장 적절한 운동능력 측정 지표는 VO2 VAT라는 내용으로 FDA와 미팅을 했고, FDA는 추가자료를 요청했다.
메지온은 NDA 신청을 위해 유데나필의 장기안전성 시험을 진행했으며 전문가들의 논문을 확보했다.
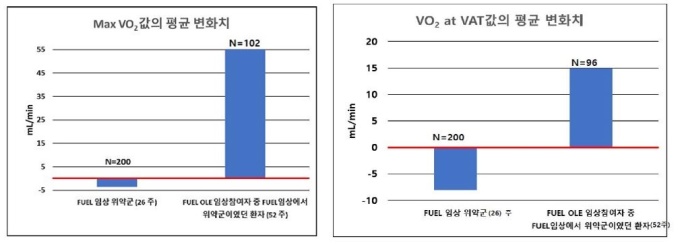
메지온이 실시한 장기안전성 시험(OLE)은 앞서 진행됐던 유데나필 글로벌 임상 3상시험(FUEL)을 완료한 환자 400명 중 장기안전성 시험을 원하는 300명을 대상으로 진행중이다. 지난해 7월 마지막 환자 등록을 완료한 후 12월까지 52주간 FUEL 임상에서 위약(가짜약)을 투여받은 환자에 유데나필을 투약한 결과 Max VO2와 VO2 VAT 두 지표 모두 약에 의한 운동 능력치가 향상된 것으로 나타났다.
또한, 메지온은 미국 소아심장네트워크(PHN) 소속 골드버그 박사 등 의사들의 집단 연구 논문에서 VO2 VAT가 단심실 환자에게 더 적절한 지표라는 내용을 다룬 논문을 확보했다.
해당 논문은 Max VO2 측정치가 하락할수록 변화폭이 좁아지기 때문에 약물을 써서 수치를 향상시킬 폭도 좁아지게 된다는 내용을 포함하고 있다. 따라서 약효를 확인하기에 적절한 지표로 사용하기에는 무리가 있지만, VO2 VAT는 나이가 들어도 수치가 잘 보존되기 때문에 약물치료 효과를 더 정확하게 확인하고 측정할 수 있다는 설명이다.
메지온 측은 "FDA가 승인을 위해 요청한 핵심자료 두 가지를 구비하고 갖추기 위해 추가 시간이 소요됐다"면서 "NDA 신청 시기는 5월 말로 예상하고 있고 승인 확률은 더 올라갔다"라고 설명했다.
메지온은 유데나필이 FDA에서 NDA 승인을 받게 되면 14~15개 보험사로부터 보험적용을 해주겠다는 응답을 받았다고 밝혔다.
메지온 측은 "단심실증은 승인된 약이 없는 아동희귀병으로, 가격을 포함해 적용범위를 결정할 때 3상에서 증명된 운동능력향상결과와 간기능저하 억제결과를 추가로 사용할 계획"이라며 "희귀병 치료제 가격은 환자 숫자와 효능에 따라 연간 5만불에서 많게는 160만불까지 책정돼 있다"라고 설명했다.
메지온이 보험코드 조회를 통해 폰탄수술 치료비 청구 대상자를 조회한 결과 지난 5년간 미국내 단심실증 환자는 7만8000여명이다. 이중 12~19세 환자는 대략 1만9000명, 19세 이상은 5000명으로 추산된다.
치료가 필요한 환자들에게 우선적으로 제공하는 조기공급프로그램(EAP)와 관련해서는 "신약 출시 전 환자를 최대한 확보하기 위한 목적이었지만, 좋은 임상자료가 나온 현 시점에서는 무리하게 강행할 필요가 없다는 입장"이라며 "의학계의 긍정적인 반응, 긍정적인 OLE 데이터 결과 등에 대한 기대감으로 유데나필의 침투율이 높을 것으로 예상된다"라고 설명했다.
allzero@newspim.com
























