[서울=뉴스핌] 정승원 기자 = 내년에 전체 진단검사로 확대되는 체외진단 의료기기 선진입 후평가 시범사업에 안전성 문제가 제기됐다.
8일 국회 보건복지위원회 윤소하 정의당 의원이 보건복지부와 한국보건의료연구원으로부터 제출받은 체외진단 의료기기 선진입 후평가 제도 진행상황에 따르면, 감염병에 대한 체외진단 의료기기 선진입 후평가 시범사업에 신청한 업체는 단 한 건이었다.
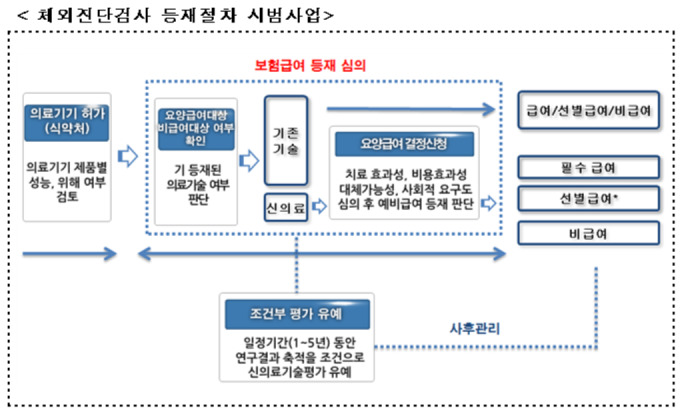
체외진단 의료기기기 선진입 후평가 시범사업은 올 12월까지 진행하고 내년부터는 모든 진단검사에 대해 확대한다는 계획인데 제대로 준비가 갖춰지지 않은 것이다.
문재인 대통령은 지난해 7월 분당서울대병원에서 의료기기 규제완화 정책을 발표했다.
이날 발표한 내용 중에는 체외진단의료기기의 경우 식품의약품안전처의 허가를 취득한 이후 시장진입까지 시간이 너무 많이 소요되고, 식약처의 허가와 보의연의 신의료기술평가가 중복규제라며 체외진단의료기기에 대한 선진입 후평가 제도가 포함됐다.
선진입 후평가가 이뤄지는 체외진단의료기기의 경우 식약처 허가를 취득한 이후 신의료기술평가를 거치지 않고 건강보험 등재 절차로 바로 진입할 수 있도록 하고 시장으로 진입해 환자에게 사용할 수 있게 했다.
새롭게 개발되는 체외진단의료기기에 대한 안전성 문제가 제기될 우려를 감안해 실시 기관을 진단검사의학과 전문의가 있는 전국 319개 종합병원급 이상으로 제한하고 감염병 진단검사에 사용되는 체외진단의료기기에 한 해 시범사업을 진행하기로 했다.
시범사업 전 복지부는 연내 최소 5건 이상 신청이 있을 것으로 예상했지만 지난 9월 시범사업 선정 확인서가 발급된 결핵균 특이항원 혈액검사 단 한 건이 전부였다.
의료기기 산업에 큰 도움이 될 것처럼 발표했지만 실제로는 시범사업조차 제대로 진행이 안 된 것이다.
윤소하 의원은 “이렇게 짧은 기간 졸속으로 진행된 시범사업을 거쳐 바로 내년 1월부터 전체 검사로 확대하는 본 사업을 추진하겠다는 것이 문제”라며 “시범사업 시행이후 1년도 안 된 시기에 적용된 사례가 단 1건인 상황에서 본사업으로 대상을 확대하는 것은 안전성 등에서 문제가 될 수 있다”고 지적했다.
기존 제한적 의료기술과 신의료기술 평가유예처럼 신의료기술평가를 거치지 않는 또 하나의 예외제도를 만드는 것이 신의료기술평가 자체를 무력화하게 된다는 지적도 나왔다.
윤 의원은 “정부의 발표 당시 체외진단의료기기의 선진입 후평가에 대한 여러 우려들이 있어 시범사업을 하기로 했던 것인데 그 문제제기가 무색하게 된다”며 “규제를 완화하는 별도 트랙을 새롭게 만드는 것은 기본 제도인 신의료기술평가를 뒤흔들 수 있다는 점에서 효과성이 분명치 않다면 원점 재검토가 필요하다”고 주장했다.
origin@newspim.com























