[서울=뉴스핌] 김신영 기자 = 의료 인공지능(AI) 전문기업 제이엘케이는 두개내출혈 검출 솔루션 'JLK-ICH'가 보완 사항 없이 미국 식품의약국(FDA) 승인(510k)을 완료했다고 6일 밝혔다.
이번 FDA 승인은 제이엘케이의 뇌졸중 AI 솔루션 중 4번째로 전체 FDA 승인 건수는 5건으로 늘어났다.
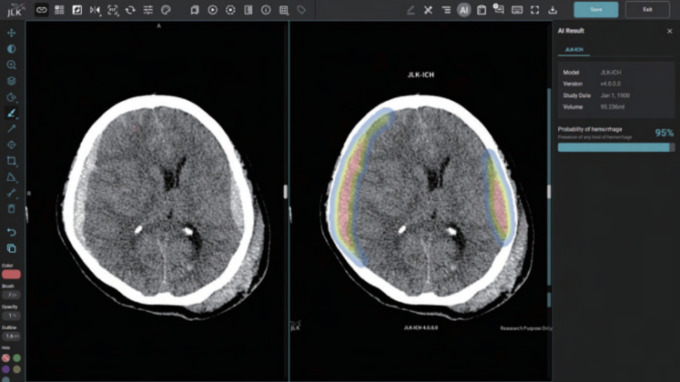
JLK-ICH는 환자의 뇌 CT 영상을 분석해 뇌출혈 영역을 검출하는 AI 솔루션으로, 응급실에서 뇌출혈 여부를 신속히 확인하는 데 쓰일 것으로 기대된다. 기존의 JLK-LVO, JLK-CTP, JLK-PWI 솔루션과 연동돼 뇌졸중 진단부터 치료 결정까지 전 과정을 지원하며, 미국 병원 시장에서의 경쟁력을 크게 높일 전망이다.
뇌출혈은 뇌경색 대비 중증도가 높아 치료 골든타임 확보가 필수적이다. JLK-ICH는 임상연구를 통해 발생 특성이 다른 5가지 뇌출혈 유형 모두에서 높은 검출 성능을 입증해 신속한 치료 결정에 기여할 것으로 보인다.
미국에서는 연간 약 8600만 건의 CT 촬영이 이뤄질 정도로 빈도가 높은 만큼 CT 영상을 기반으로 한 JLK-ICH의 시장성은 높을 것으로 보인다.
제이엘케이는 올해도 미국 FDA와 일본 PMDA를 중심으로 글로벌 인허가 활동에 주력할 계획이다. FDA에는 추가로 6개의 솔루션 인허가를 신청하고, 일본에서는 8개의 솔루션에 대한 인허가를 진행할 예정이다. 또한 각국 보험수가 적용을 통해 해외 매출 발생에 속도를 낼 방침이다.
김동민 제이엘케이 대표는 "보완사항 없이 단번에 승인을 마친 이번 FDA 획득으로 제이엘케이가 자체적으로 구축한 인허가 역량의 우수성을 입증한 만큼 남은 인허가와 현지 보험수가 획득에 주력해 성공적인 해외 진출 성과를 가져오는 최선을 다하겠다"고 말했다.
sykim@newspim.com























