[서울=뉴스핌] 정경환 기자 = 셀리버리는 약리물질 생체 내 전송기술인 TSDT 플랫폼을 활용해 파킨슨병 치료제로 개발 중인 'iCP-Parkin'의 알츠하이머병 치료효능기전 증명에 성공했다고 10일 밝혔다.
앞서 셀리버리는 지난 2월 알츠하이머병 동물모델에서 iCP-Parkin 투여 시 인지기능이 96% 개선됐다고 밝힌 바 있다.
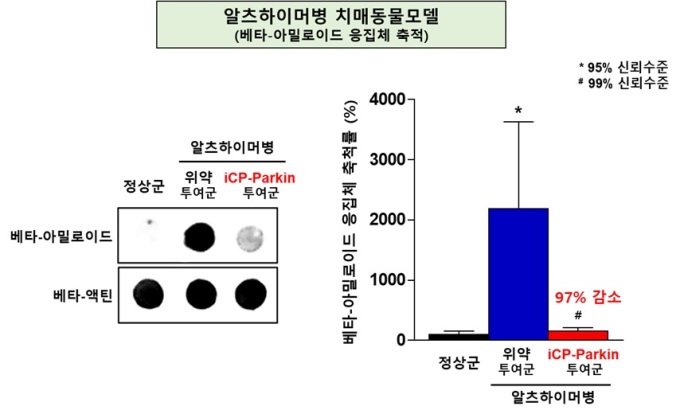
회사 관계자는 "분석 결과, iCP-Parkin이 치매를 유발하는 원인으로 지목되는 베타-아밀로이드 응집체를 97%까지 제거해 기억력 및 판단력을 나타내는 인지기능을 알츠하이머병 발병 이전 수준으로 회복(96%)시킬 수 있다는 치료효능 기전을 증명하게 됐다"고 설명했다.
셀리버리에 따르면, 기존에 알려진 퇴행성뇌질환 치료 후보물질들은 낮은 혈뇌장벽 투과율 때문에 뇌신경세포 내부에 직접 전송되지 못 해 근본적인 치료제로서 한계가 있었다. 일반적으로 알려진 단일항체 및 이중항체 치료제들은 혈뇌장벽 투과율이 각각 약 0.1~0.2% 그리고 최고 0.5% 정도로, 퇴행성뇌질환 치료제로 개발 중인 항체치료제들은 많은 양을 투약해도 여전히 치료효능이 낮다는 게 일반적 평가다.
하지만, iCP-Parkin은 아두카누맙과 동일한 베타-아밀로이드 응집체 제거(97%) 기전과 뇌신경세포 보호효능을 가지고 있을 뿐만 아니라, 분자 크기가 큰 재조합단백질 치료제임에도 불구하고 TSDT 플랫폼기술을 활용함으로써 혈뇌장벽 및 뇌신경세포 투과성이 일반 단일항체 치료제보다 높다.
회사 관계자는 "iCP-Parkin은 알츠하이머병 동물모델에서 1차 혈뇌장벽 투과율 분석 결과, 약 3%의 뛰어난 혈뇌장벽 투과율을 보였다"면서 "이는 일반 항체치료제들과 비교 시 최대 약 30배 이상의 전송능력 차이를 보이는 결과"라고 했다. 이어 "이를 좀 더 확실히 하기 위해 현재 영국에서 각각 150개의 알츠하이머병 치매동물의 뇌와 혈액샘플을 대상으로 계속해서 정밀 분석 중"이라며 "여러 데이터를 종합할 때 (투과율이) 10% 안팎 수준이 될 것으로 기대한다"고 덧붙였다.
한편, 지난 7일 미국 식품의약국(FDA)은 바이오젠의 알츠하이머병 치료제 아두카누맙(Aducanumab)을 베타-아밀로이드에 특이적으로 결합해 제거하는 기전을 가진 단일항체로서 첫 조건부 판매를 승인했다.
회사 관계자는 "(바이오젠이) 임상시험에서 일부 초기 알츠하이머병 환자에게 고용량을 투여하면 사고능력과 인지기능이 23% 개선됐고, 베타-아밀로이드 응집체가 약 60% 감소됐다고 밝혔으나, FDA가 임상 4상에서 결과를 얻지 못 하면 승인을 취소할 수 있다고 한 만큼, 아두카누맙의 효력을 뛰어넘는 차세대 알츠하이머병 치료제 개발이 여전히 절실한 상황"이라고 했다.
그러면서 "글로벌 제약사들로부터 TSDT 플랫폼 기반 혈뇌장벽 투과기술에 대해 심도있는 논의 요청이 와 있다"며 "이달 14일부터 18일까지 진행되는 '바이오 인터내셔널 2021'에서 오랫동안 글로벌 제약사들이 요구했던 이 혈뇌장벽 투과능 분석 결과를 바탕으로 TSDT 플랫폼 기술과 iCP-Parkin의 라이센싱을 적극 추진할 계획"이라고 덧붙였다.
hoan@newspim.com























