EC-18 활용한 코로나19 치료제 한미 임상2상 중
올 1,2분기 내 임상 종료 계획..자체 생산 가능
[서울=뉴스핌] 서영욱 기자 = 롯데그룹이 바이오산업 진출을 선언하면서 파트너로 점찍은 엔지켐생명과학에 관심이 집중되고 있다.
엔지켐생명과학은 '캐시카우' 역할이 가능한 위탁생산(CMO) 사업은 물론 코로나19 치료제와 항암제 등 신약개발에 몰두하고 있어 성장 가능성에 높은 평가를 받았다는 분석이다. 엔지켐은 충청북도 오송에 신축공장을 세워 생산 물량을 늘릴 계획으로, 코로나 치료제 임상 2상이 통과되면 자체 생산이 가능한 시스템을 구축하고 있다.
25일 제약바이오업계에 따르면 엔지켐생명과학은 지난 1999년 설립된 글로벌 신약개발 벤처기업으로, 제천에 2개의 GMP 생산공장과 글로벌 신약개발연구소를 갖추고 있다.
 |
2010년 브리짓라이프사이언스가 인수한 후 2013년 코넥스에 상장됐고, 2018년 기술특례를 통해 코스닥으로 이전 상장했다. 24일 기준 시가총액은 9936억원으로, 코스닥 상장사 중 62위다. 지난해 매출액은 258억원, 191억원의 영업손실을 기록했다. 대표이사는 브리짓라이프사이언스의 회장인 손기영씨다.
매출 대부분은 원료의약품 생산으로 이뤄진다. 항응고제(19.94%), 진해거담제(16.57%), 위궤양치료제(6.80%) 순으로 매출 비중이 높다. 제천에 이어 충북 오송에서 1만7499㎡ 규모의 제조공장을 신설하고 있다.
엔지켐은 2004년부터 천연물 녹용에서 유래한 신약물질인 '모세디피모드(EC-18)'를 활용해 다양한 신약을 개발하고 있다. 항암제로 유발되는 호중구감소증 치료제와 패혈증, 류마티스관절염, 천식, 아토피피부염 치료제 등이다.
호중구감소증과 항암화학방사선 치료 유발 구강점막염(CRIOM)은 임상 2상 종료 후 혁신신약 지정을 목표로 하고 있다. 특히 CRIOM은 미국 식품의약국(FDA)으로 부터 신속심사 지정을 받아 혁신신약 지정 가능성이 높다는 게 회사의 설명이다.
또 EC-18은 급성방사선증후군(ARS) 치료제로서 지난 2017년 말 FDA로부터 희귀질환치료제로 지정을 받았다. 현재 미국에서 임상 2상에 상응하는 비임상 효능 시험을 진행하고 있으며, 연내 시험을 완료하고 판매 허가 신청을 진행할 예정이다.
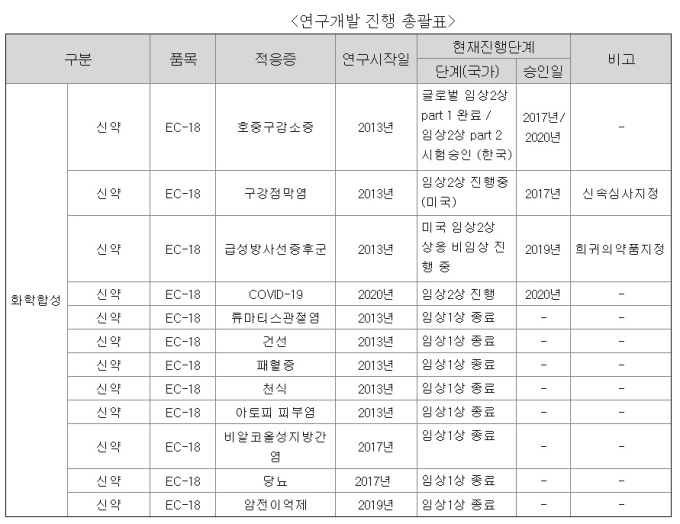
특히 엔지켐은 EC-18을 코로나19 치료제로도 개발하고 있어 주목을 받고 있다. 엔지켐에 따르면 EC-18은 비임상연구를 통해 중증환자에게서 나타나는 급성 폐손상, 급성 호흡곤란, 패혈증 등의 치료효과를 증명한 바 있다.
이를 계기로 지난해 5월 식약처로부터 임상 2상 승인 받아 충북대병원, 인천의료원, 인하대병원 등에서 임상시험을 진행하고 있다. 미국에서도 지난해 8월 임상 2상 승인을 받아 임상시험이 진행 중이다. 엔지컴은 올 1,2분기에 각각 한국과 미국의 임상 2상을 완료한다는 방침으로, 긴급사용승인(EUA) 또는 조건부허가 승인을 제출할 예정이다.
엔지켐 측은 "치료제로서 EC-18은 바이러스에 의한 폐렴을 신속히 치료 및 종결하는 기전이기 때문에 바이러스의 변이 또는 신종바이러스의 출현과 관계없이 사용 가능한 장점이 있다"고 설명했다.
제약업계 관계자는 "임상 2상 성공 후 EUA 획득 시 제천공장에서 대량 생산과 판매가 가능한 인프라를 구축하고 있다"고 설명했다.
syu@newspim.com























