[서울=뉴스핌] 심지혜 기자 = SK 자회사 SK바이오팜이 독자 개발한 뇌전증 치료제 엑스코프리(세노바메이트정)가 미국 식품의약국(FDA)의 시판 허가를 받았다. 이는 대한민국 최초로 독자개발한 신약이라는데 의미가 있다.
신약 개발은 통상 10~15년의 기간과 수천억원 이상의 비용이 투입되는데다 5000~1만개의 후보물질 중 단 1~2개만 신약으로 개발돼 성공 확신이 어렵다. 이에 이번 SK바이오팜의 신약 개발에는 최태원 SK회장의 의지가 뒷받침됐기에 가능했다는 평가가 나온다.

22일 SK바이오팜은 뇌전증 치료제 엑스코프리가 미국 FDA로부터 신약승인을 받았다고 밝혔다. 특히 국내 제약사가 후보물질 발굴부터 임상개발, 신약허가까지 전 과정을 독자적으로 수행해 FDA 승인을 받은 것은 대한민국 최초다.
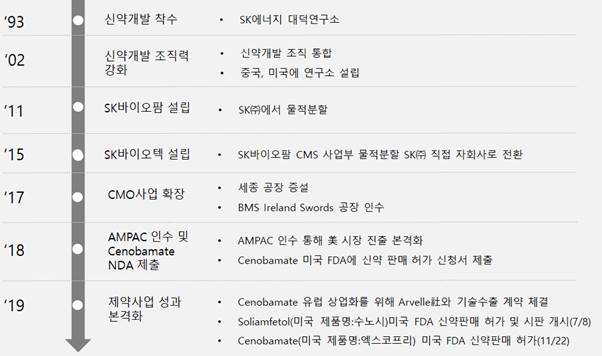
SK바이오팜의 시작은 SK가 1993년 대덕연구원에 연구팀을 꾸리면서 불모지와 같았던 제약사업에 발을 들이면서부터다. 인구 고령화 등으로 바이오∙제약 사업은 고부가 고성장이 예상되는 영역인데다, 한국에서는 글로벌 시장에 자체개발 신약이 없었다. 국내 제약시장이 복제약 위주로 형성돼 있지만 SK바이오팜은 혁신 신약개발에 몰두했다.
2002년 최 회장은 바이오 사업의 꾸준한 육성을 통해 2030년 이후에는 바이오 사업을 그룹의 중심축 중 하나로 세운다는 장기 목표를 제시했다. 신약 개발에서 의약품 생산, 마케팅까지 모든 밸류체인을 통합해 독자적인 사업 역량을 갖춘 글로벌 바이오∙제약 기업을 키워낸다는 비전이었다.
같은 해 생명과학연구팀, 의약개발팀 등 5개로 나누어져 있던 조직을 통합, 신약 연구에 집중케 하는 한편, 다양한 의약성분과 기술 확보를 위해 중국과 미국에 연구소를 세웠다.
2007년 지주회사 체제 전환 이후에도 신약개발 조직을 따로 분사하지 않고 지주회사 직속으로 둬 그룹 차원에서 투자와 연구를 지속하게 한 것도 신약 개발 의지가 배경이 됐다는 설명이다. 단기 실적 압박에서 벗어나 지속적인 투자와 장기적인 비전이 담보돼야 가능하다는 판단에서다.
이후 SK는 수천억 규모의 투자를 지속했다. 임상 1상 완료 후 존슨앤존슨에 기술수출 했던 SK의 첫 뇌전증치료제 '카리스바메이트'가 2008년 출시 문턱에서 좌절됐지만 투자는 그치지 않았다. 같은해 SK바이오팜의 미국 현지법인 SK라이프사이언스의 R&D 조직을 강화하고 업계 전문가들을 채용함으로써 독자 신약 개발을 가속화 했다. 이때 역량을 강화했던 SK라이프사이언스가 이번에 FDA 승인을 얻은 엑스코프리의 임상을 주도했고, 발매 이후 미국 시장 마케팅과 영업까지 도맡을 예정이다.
이후 SK는 신약 개발 사업의 집중 육성을 위해 2011년 사업 조직을 분할해 SK바이오팜을 출범시켰다. SK바이오팜은 이를 바탕으로 FDA가 요구하는 기준에 맞춰 뇌전증 치료제 개발에 성공했다.
전세계 뇌전증 치료제 시장은 2018년 61억달러(약 7조1400억원) 규모로 2024년까지 70억 달러(약 8조2000억원) 규모의 성장이 예상된다(Frost & Sulllivan, 2019). SK는 엑스코프리로부터 발생되는 수익을 기반으로 제2, 제3의 글로벌 혁신신약 개발을 지속할 방침이다.
이항수 SK수펙스추구협의회 PR팀장은 "SK의 신약개발 역사는 리스크를 두려워하지 않고 새로운 도전을 거듭해 혁신을 이뤄낸 대표적 사례"라며 "명실상부한 글로벌 제약사의 등장이 침체된 국내 제약사업에 큰 자극이 될 것"이라고 말했다.
sjh@newspim.com























