감염병 체외진단검사 건강보험등재 390일→140일
[세종=뉴스핌] 임은석 기자 = 4월부터 안전성 우려가 적은 감염병 체외진단기기에 대해 선 진입, 후 평가 방식을 적용해 빠르게 시장으로 진입할 수 있는 길이 열린다. 또한 감영병 체외진단검사의 건강보험등재 절차고 390일에서 140일로 간소화 된다.
보건복지부는 지난해 7월 19일에 발표했던 '의료기기 규제혁신 및 산업육성방안'의 후속조치로, '감염병 체외진단검사의 건강보험 등재절차 개선 시범사업'을 내달 1일부터 실시한다고 31일 밝혔다.
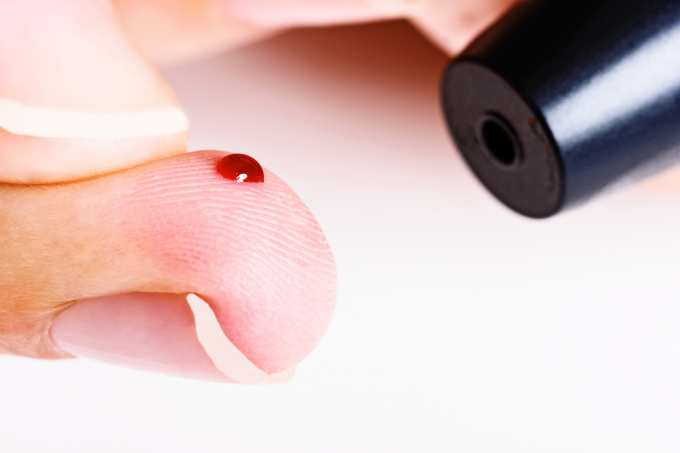
체외진단검사분야는 사람의 몸 밖에서 질병을 진단하기 때문에 비교적 안전한 의료기술로 평가받고 있다. 실제로 체외진단기기는 새로운 의료기술의 안전성·유효성을 논문 등을 토대로 검증하는 신의료기술평가에서 안전성 문제로 인해 탈락한 사례가 없다.
이번 시범사업에서는 식품의약품안전처 허가를 통해 의료기기의 안전성을 검증받은 감염병 체외진단검사에 대해 신의료기술평가 없이 곧바로 건강보험에 등재할 수 있도록 지원할 방침이다. 이에 따라 지금까지 390일이 걸리던 건강보험등재 기간이 140일로 줄어든다.
시범사업 대상은 콜레라, 장티푸스, A형 간염 등 법정 감염병을 진단하는 체외진단검사이며, 관련 서류를 갖출 경우 신의료기술평가 없이 건강보험 등재 신청이 가능해진다.
감염병 체외진단검사는 감염여부만을 진단하는 검사로서, 다른 검사에 비해 진단결과가 간단·명료해 관리·감독이 쉬운 편이다.
이에 따라 감염병 체외진단검사부터 건강보험 등재 절차를 개선한 후, 하반기에는 법령 개정 등을 통해 체외진단검사 전체를 대상으로 본 사업을 확대·시행할 계획이다.
시범사업은 선 진입하는 의료기술에 대한 사후관리·감독 체계를 점검하기 위해 진단검사의학과 전문의 또는 병리과 전문의가 근무하는 종합병원급 이상 의료기관에서 우선 실시한다.
시범사업 기간 동안 신청인은 한국보건의료연구원에 의료현장 활용 결과를 분기별로 보고해야 하고, 이를 토대로 신의료기술평가위원회는 관리·감독과 1~5년 후 신의료기술 승인여부를 결정한다.
시범사업 신청은 내달 1일부터 한국보건의료연구원에서 받는다. 신청인은 감염병 체외진단검사 시범사업의 신청서 등을 작성해 한국보건의료연구원 신의료기술평가사업본부 전자우편과 우편을 통해 접수할 수 있다.
손호준 복지부 의료자원정책과장은 "감염병 체외진단검사의 건강보험 등재절차 개선 시범사업을 통해 기존에 오랜 시간이 걸리던 의료기기 시장 진입 절차를 보다 합리적으로 개선해 나갈 것"이라며 "이번 시범사업을 통해 관리·감독 체계를 점검하여 하반기 예정된 본 사업을 조속히 추진할 것"이라고 전했다.
fedor01@newspim.com