코오롱생명과학·신라젠 등 임상3상 진행 중
대부분 ‘벤처’...생산·연구시설·상업화 전략 보조 시급
[뉴스핌=박예슬 기자] 국내 제약업계가 새로운 블루오션인 '유전자 치료제' 시장에서 바쁜 걸음을 옮기고 있다. 국내뿐 아니라 세계적으로도 진출 사례가 많지 않은만큼, 국내 제약사들의 선점이 기대되는 종목이다.
2일 업계에 따르면 5000억원대 기술수출을 이뤄낸 코오롱생명과학을 비롯해 툴젠, 신라젠, 바이로메드, 제넥신 등의 바이오벤처 기업들이 국내외에서 유전자 치료제 임상을 진행 중이다. 특히 상당수 파이프라인이 임상3상 단계를 앞두거나 돌입해 수년 내 시장 출시도 기대된다.
 |
| <사진=게티이미지> |
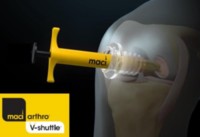
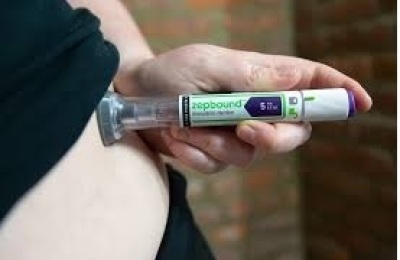
유전자 치료제란 질병 치료 및 예방의 목적으로 인체에 투입하는 유전물질을 함유한 의약품이다. 결함이 있어 질병을 일으키는 유전자를 정상적으로 교정, 교체함으로서 질병을 근본적으로 치료한다.
국내 첫 유전자 치료제 ‘인보사(제품명 티슈진-C)’ 출시가 기대되는 코오롱생명과학은 2017년 출시를 앞두고 생산시설 확충까지 계획하고 있다.
코오롱생명과학 관계자는 “현재 충주공장에서 주사제 1만 도즈를 생산할 수 있는 시설을 보유하고 있으며 오는 2019년까지 추가로 5만 도즈 규모의 생산시설을 확충할 계획”이라고 말했다.
이 회사에 따르면 신규 생산시설의 위치는 확정되진 않았으나 현재 있는 충주공장 인근이 유력하다. 이곳에서 생산된 주사제는 국내시장과 중국, 일본에 수출한다. 현재 임상3상중인 미국 임상이 완료하고 출시가 확정되면 미국 수출 분량까지도 일부 생산하게 된다.
신라젠도 간암 유전자치료제인 ‘펙사벡(JX-594)’에 대해 미국, 대만, 뉴질랜드에서 임상3상을 진행 중이다. 국내에서는 12개 병원에서 임상 시험을 진행할 예정이다.
펙사벡은 우두바이러스 유전자를 조작해 환자의 암세포만 감염시켜 체내 면역체계를 활성화시키는 방식으로 암을 파괴하는 원리다.
바이로메드도 유전자 치료제인 당뇨병성 신경병증 치료제 ‘VM202-DPN’은 미국 임상3상이진행중이며 허혈성 지체질환 치료제 ‘VM202-PAD’도 미국 임상3상 승인을 받고 올 4분기부터 착수 예정이다.
이밖에 근위축성 측삭경화증 치료제 ‘VM202-ALS’는 미국 임상 1/2상을 완료하고 2상을 준비하고 있다.
‘유전자 가위’ 원천기술을 갖고 있는 툴젠(대표 김종문)도 주목받고 있다. 지난 9월 유전자 가위 관련 기술인 크리스퍼 원천기술에 대한 국내 특허를 받고 상업화를 준비 중이다.
툴젠의 유전자 가위 기술은 희귀질환인 ‘샤르코-마리-투스’나 혈우병 등 난치성 유전질환을 치료하는 데 쓰인다. 질병을 일으키는 잘못된 유전자 배열을 유전자 가위로 올바르게 교정하는 원리다.
다만 유전자 가위 기술을 활용한 치료제의 임상 돌입은 2018년 이후로 현재까지는 전임상 단계다.
한편, 유전자 치료제 개발에 도전하는 대부분의 제약사들이 소규모 벤처 기업인 만큼 상업화 전략이 취약하고 관련 연구·생산시설이 부족하다는 지적도 있다.
현재 국내 유전자치료제 전문 생산시설은 충북 오송과 전남 화순 두 곳에만 있다. 현행법상 국내 생산시설이 부족할 경우 외국 CMO를 이용할 수 있으나 장기적으로 자체 생산시설을 확충해야 한다는 것.
곽수진 한국보건산업진흥원 제약산업지원단 연구원은 “코오롱생명과학을 제외한 유전자 치료제 개발기업들은 소규모의 벤처이기 때문에 자체 생산시설을 보유하고 있지 않다”며 “상업화 경험이 없는 벤처라서 전략에도 취약하다”고 말했다.
곽 연구원은 이에 따라 “국내 유전자 치료제 개발 기업들의 글로벌 진출을 활성화하기 위해 위탁연구 및 생산시설 확충, 전문인력 확보, 글로벌 시장에서의 마케팅 전략 수립이 시급하다”고 덧붙였다.
[뉴스핌 Newspim] 박예슬 기자 (ruthy@newspim.com)
 영상
영상