[서울=뉴스핌] 박다영 기자 = 헬릭스미스가 약물 혼용으로 임상 3상 결과 발표를 미룬 당뇨병성 신경병증 치료제 엔젠시스(VM202)의 유효성과 안전성을 확인했다며 '미완의 성공'이라고 자평했다.
헬릭스미스는 25일 '헬릭스미스 주주님들께'라는 뉴스레터를 통해 "이번 3상을 '미완의 성공'으로 자평했다"며 "임상 2상 때보다 훨씬 더 큰 규모에서 유효성과 안전성을 확인했다"고 밝혔다.
임상 3상 과정에서 위약군(가짜약)과 실험약을 혼용한 환자를 제외하면 통계적으로 유의미한 결과가 도출됐으며 완치 환자가 있다는 이유에서다.
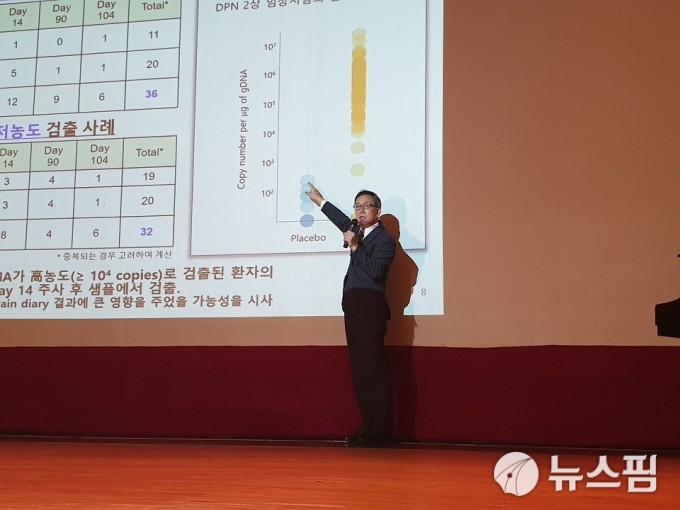
헬릭스미스에 따르면 임상 3상 대상자 중 약물 혼용이 의심되는 환자를 제외한 438명의 통증 감소 효과를 연구한 결과 p값이 3개월에서 0.0089, 6개월에서 0.0018로 나왔다. p값은 통계적 유의성을 의미하며, 0.05 이하면 통계적으로 유의미하다고 간주한다.
또, 438명 중 VM202를 투약하고 6개월 간 통증일기를 기록한 환자 중 14명이 완치됐다. 위약군에서는 2명이 완치된 것으로 나타났다. 이는 각 집단에서 4.7%, 1.5%에 해당하는데 회사 측은 이번 VM202가 다른 진통제 임상보다 완치 환자 비율이 높다고 풀이했다.
이 같은 사실을 종합해 헬릭스미스는 "VM202의 약물 효과는 자신한다"고 강조했다.
회사 측은 "소규모 임상 3상을 2~3개 진행해 2021년 종료해 신약허가신청(BLA)을 제출하고 향후 임상은 정확히 끝내도록 최선을 다하겠다"고 했다.
allzero@newspim.com























