[서울=뉴스핌] 정승원 기자 = 식품의약품안전처(처장 이의경)와 한국보건의료연구원(원장 한광협)은 신개발의료기기의 신속한 시장진입 지원체계 구축을 위해 식약처의 허가도우미와 보의연의 신의료기술평가를 시범 연계 운영한다고 27일 밝혔다.
허가도우미는 신개발의료기기 등 제품 개발부터 허가에 이르는 과정에서 필요한 기술적·행정적 지원을 맞춤형으로 실시하는 제도로 지금까지 총 31개 제품이 허가됐다.
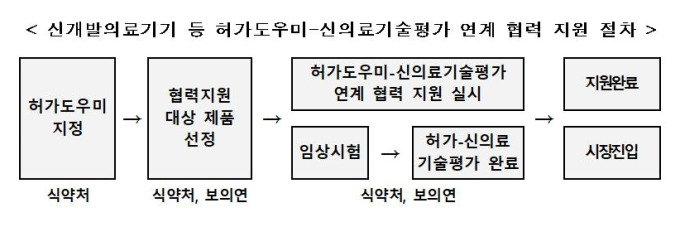 |
| [이미지= 식품의약품안전처] |
지원사업은 허가도우미로 지정된 3개 분야에 대해 27일부터 시행되며 ▲허가단계부터 신의료기술평가를 고려한 임상 설계 ▲개발제품 사용목적 구체화 ▲제조 및 품질관리시스템(GMP) 검토 ▲안전성 및 성능 검토 등 전주기 컨설팅 등을 실시할 계획이다.
특히 '임상시험 설계 자문'을 통해 허가를 위한 임상시험 계획 설계단계에서 신의료기술평가를 동시에 고려할 수 있어, 신의료기술평가 시 안전성·유효성 연구결과의 미흡으로 시장진입이 어려워지는 것을 해소할 수 있을 것으로 예상된다.
그 동안 기술력은 있으나 영세한 업체는 전문인력이나 정보 부족으로 신의료기술 등재를 거쳐 시장 진입하는데 어려움을 겪었다.
실제로 의료기기 허가 후 신의료기술 등재를 통한 시장진입 비율은 36.2%로 나타났다.
식약처와 보의연은 "이번 협력사업으로 신개발의료기기의 시장진입 기회가 확대될 것"이라며 "원활히 운영될 수 있도록 노력할 것"이라고 밝혔다.
origin@newspim.com
 영상
영상