정부 2015년 "세계 5대 임상시험 강국으로 도약하겠다"
전문가 "안전대책 미흡한데 임상시험 건수 경쟁 벌이는 것 위험해"
[편집자주] 지난해 서울의 임상시험 도시 점유율은 세계 1위, 국내 전체로 따졌을 때 한국은 세계 6위에 이름을 올리고 있다. 정부는 지난 2022년까지 임상시험 5대 강국에 진입하겠다며 관련 규제는 완화하고 지원은 늘려 왔다. 그 결과, 대한민국은 다국적 제약사의 ‘임상시험’ 놀이터가 됐다. 임상시험의 위험성, 그리고 임상시험 산업육성이라는 포장지에 감춰진 정부와 다국적 제약사의 실태를 추적한다.
[서울=뉴스핌] 임성봉 기자 = 정부는 세계 임상시장 규모가 커지고 있다며 임상 산업 육성에 집중하고 있다. 그러나 임상시험은 심하면 사망까지 이를 수 있는 부작용이 있는 것도 현실이다.
따라서 구제 시스템과 안전망 구축 등이 먼저 이루어져야 한다는게 전문가들의 주장이다. 정부가 부실한 생명윤리위원회(IRB) 구성, 미흡한 구제방안을 정비하지 않은채 임상시험을 권장하는 것은 문제라는 지적이다.
◆브레이크 없는 정부의 임상시험 유치 정책
정부가 국내 임상시험 산업을 활성화하기 시작한 것은 2000년대 초반이다. 당시 국회 보건복지위원회에서 “국내 신약개발의 해외 임상시험 의존도가 지나치게 높다”는 지적이 나오면서 정부는 임상시험 인프라 구축에 첫발을 뗐다.
이후 보건복지부는 관련 인프라를 구축하기 위해 2004년 국가임상시험사업단(현 한국임상시험산업본부)을 출범하고 지역별 임상시험센터도 건립했다. 현재 지역별 임상시험센터는 서울대병원 등 14곳에 이른다.
하지만 당초 정부의 정책 의도와는 달리 국내 제약사가 신약개발 역량이 기대에 못 미치면서 이들 인프라는 다국적 제약사의 차지가 됐다.
정부는 결국 정책 방향을 선회해 2012년 서울아산병원, 서울대병원을 시작으로 임상시험 글로벌선도센터를 지정했다. 다국적 제약사의 국내 임상시험을 유치하기 시작한 것이다.
 |
| 보건복지부가 2015년 발표한 '임상시험 글로벌 경쟁력 강화방안' 자료 [사진=보건복지부] |
이런 가운데 정부는 2015년 8월 “2020년까지 세계 5대 임상시험 강국으로 도약하겠다”며 ‘임상시험 글로벌 경쟁력 강화방안’을 발표, 본격적으로 다국적 제약사에 대한 임상시험 지원을 강화해 나갔다.
정부는 “치열한 글로벌 임상시험 경쟁에 능동적으로 대응, 그동안 발전된 인프라를 바탕으로 글로벌 임상강국 도약을 위한 추가적인 모멘텀을 마련해야 한다”고 임상산업 육성의 필요성을 밝혔다. 이후 정부는 글로벌 임상시험 유치 활성화 등 6가지 추진과제를 세우고 본격적으로 임상 산업 육성에 나섰다.
또 보건복지부는 2015년 이후 임상시험 승인 절차를 간소화하고 다국적 제약사에게 국내 임상시험 승인 절차를 돕는 ‘원스톱’ 서비스 등을 제공하면서 국내 임상시험 유치에 박차를 가하고 있다.
이 같은 정책흐름과 국내 임상시험 건수를 교차 분석해보면 2001년 18건에 불과했던 다국적 제약사의 임상시험은 국가임상시험사업단이 출범한 2004년 95건으로 치솟는다. 이 수치는 임상시험 글로벌선도센터를 운영한 2012년에 303건을 기록, 현재까지 비슷한 수준을 유지하고 있다.
◆“정부, 임상시험 건수에만 목매고 있다”
전문가들은 정부가 국민의 안전이 달린 ‘임상시험’을 대대적으로 유치하면서 향후 큰 사회적 후유증을 남길 수 있다고 경고한다. 특히 임상시험에 대한 안전대책이 미흡한 상황에서 단순히 실적 경쟁을 벌이는 것 아니냐는 우려의 목소리가 높다.
보건복지부 산하 한국임상시험산업본부는 지난해 상반기 세계 임상시장 분석 결과를 내놓으며 “임상시험 승인시간 예측성 확보 및 단축, 관세 면제, 인센티브 등 임상시험을 활성화하기 위한 정부 차원의 지원을 통해 경쟁력 있는 임상시험 환경조성이 필요하다”며 정부의 추가 지원을 요구했다.
이에 따라 세계 임상 시장에서 점유율을 높이기 위해 올 하반기 정부의 대대적인 정책적 지원이 예상되면서 우려의 목소리가 높아지고 있다.
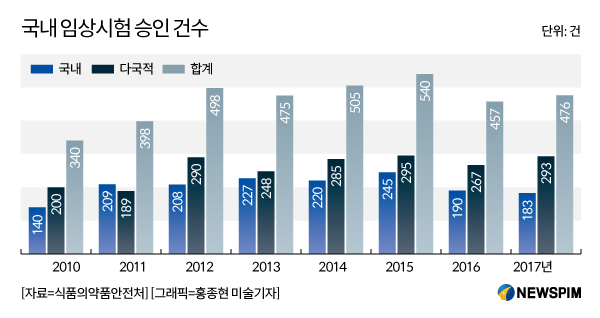 |
| 최근 국내 임상시험 승인건수 [사진=식품의약품안전처] |
김남희 참여연대 조세복지팀장은 “부작용과 효과가 입증되지 않은 약을 사용한다는 점에서 임상시험은 필연적으로 위험이 수반될 수밖에 없다”며 “이를 산업적으로 육성하는 정부의 시각은 국민의 안전이 아닌 경제적 이익만을 생각한 근시안적 시각”이라고 평가했다.
김명희 국가생명윤리정책원 사무총장은 “다국적 제약사가 단순히 국내 임상시험 인프라나 정부의 지원을 노리고 한국을 찾는 건 아니다”며 “임상시험 중에 문제가 일어나도 별다른 패널티를 받지 않으니 안심하고 오는 측면도 있다는 점을 정부가 알아야 한다”고 말했다.
김재천 건강세상네트워크 운영위원은 “임상산업 육성이 필수적인 상황이라면 국내 임상시험 안전망부터 정비했어야 했는데 정부가 이런 과정 없이 무차별적으로 임상시험만 유치하고 있다”며 “이대로라면 임상시험 부작용으로 인한 피해자가 크게 늘어날 수밖에 없다”고 지적했다.
imbong@newspim
 영상
영상